CRISPR技术革新 攻克镰刀型细胞贫血症的细胞治疗新前沿
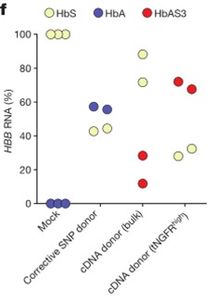
镰刀型细胞贫血症是一种由单基因突变引起的遗传性血液疾病,全球影响着数百万人。传统的治疗方法主要集中于症状管理和并发症预防,难以根治。以CRISPR-Cas9为代表的基因编辑技术,结合先进的细胞技术,为这一顽疾的治愈带来了革命性的希望,开启了精准医疗的新篇章。
CRISPR技术的原理与应用潜力
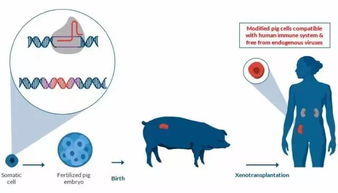
CRISPR-Cas9系统源自细菌的适应性免疫机制,能够像“分子剪刀”一样,在基因组特定位点进行精确切割。对于镰刀型细胞贫血症,其病因是HBB基因上的一个点突变(导致β-珠蛋白第6位谷氨酸被缬氨酸取代)。CRISPR技术的核心策略是直接纠正患者造血干细胞中的这个致病突变,或者通过激活胎儿血红蛋白(HbF)的表达来补偿缺陷的成人血红蛋白功能。
细胞技术的核心作用:从体外编辑到体内回输
成功的基因治疗离不开细胞技术的支撑。整个研发和应用流程通常包括以下几个关键步骤:
- 细胞采集与分离:从患者体内获取自体造血干细胞(HSCs),通常通过骨髓穿刺或外周血动员后采集。
- 体外培养与扩增:在符合GMP标准的洁净实验室中,对HSCs进行培养,确保其活性和数量满足编辑需求。
- 精准基因编辑:利用CRISPR系统(通常通过电穿孔或病毒载体递送)对培养中的HSCs进行基因修正。目前主流策略有两种:一是直接修正HBB基因突变;二是靶向抑制BCL11A基因(HbF表达的抑制因子),从而重新激活胎儿血红蛋白的生产。
- 质量控制与安全评估:对编辑后的细胞进行严格检测,确保编辑效率、目标特异性(避免脱靶效应),并清除任何未编辑或可能癌变的细胞。
- 患者预处理与细胞回输:患者首先接受清髓性化疗,清除自身有缺陷的造血系统,为编辑后的健康HSCs“腾出空间”。这些“修复好”的干细胞通过静脉输注回患者体内。
- 植入与监测:回输的HSCs在患者骨髓中定植并重建健康的造血系统,持续产生正常的红细胞。患者需接受长期随访,监测治疗效果、安全性以及是否产生持久疗效。
研发进展与临床突破
全球多个团队在此领域取得了里程碑式的成果。最著名的案例之一是名为“exa-cel”的疗法(基于CRISPR编辑BCL11A增强子)。临床试验结果显示,绝大多数接受治疗的重症镰刀型细胞贫血症患者实现了血管闭塞危象的完全消除,并持续产生高水平的胎儿血红蛋白,效果显著且持久。这标志着基于CRISPR的细胞疗法从概念走向了现实。
面临的挑战与未来展望
尽管前景光明,但该领域仍面临诸多挑战:
- 技术挑战:提高编辑效率与特异性,确保绝对安全,避免脱靶效应和染色体异常。
- 制造与成本挑战:个性化细胞疗法的制备过程复杂、耗时且极其昂贵,如何实现标准化、规模化生产以降低成本是普及的关键。
- 可及性与伦理:确保全球患者,特别是发展中国家患者,能够公平地获得这种尖端治疗。
随着CRISPR工具本身的不断进化(如更精准的碱基编辑、先导编辑技术的出现),以及细胞培养、递送技术的优化,针对镰刀型细胞贫血症的基因编辑疗法将变得更加安全、高效和可及。它不仅是单一疾病的突破,更为代表性的单基因遗传病乃至更复杂疾病的细胞治疗铺平了道路,预示着医学正步入一个能够直接改写生命源代码的新时代。
如若转载,请注明出处:http://www.tongshengbiotechnology.com/product/10.html
更新时间:2026-04-22 11:39:32